revmatoidní artritida

Revmatoidní artritida (RA), odborně arthritis rheumatica, je systémové zánětlivéautoimunitní onemocnění, které vede k chronickému zánětu synoviální tkáně, což má za následek nevratné poškození chrupavek a kostí kloubů. RA ovšem nepostihuje jen klouby, ale může vést i k závažným extraartikulárním projevům, kdy zánět může zasáhnout i oči, srdce a plíce a vést ke kardiovaskulárním a respiračním onemocněním.
RA je spojena se zvýšenou mortalitou, ke které velkou měrou přispívají právě kardiovaskulární choroby. Prevalence RA se pohybuje okolo 0,5–1 %. RA postihuje ženy přibližně 2–3krát častěji než muže.
Významnou měrou zapříčiňuje pracovní neschopnost. Je spojena s chronickou bolestí, ztuhlostí a zvýšenou úmrtností. Často má trvalé následky a pacienti mají sníženou schopnost vykonávat některé běžné činnosti, čímž se snižuje kvalita jejich života.
Rizikové faktory
Rizikové faktory se dělí na genetické a environmentální.
Genetické rizikové faktory
Bylo identifikováno více než 100 lokusů spojených s rizikem RA. Rizikové jsou některé alely hlavního histokompatibilního komplexu II. třídy (MHC II), například alely HLA-DR1 a HLA-DR4. Na těchto HLA-DR alelách se nachází tzv. sdílený epitop, což je konzervovaná sekvence 5 aminokyselin, nacházející se ve třetí hypervariabilní oblasti na pozici 70–74 na β1 řetězci těchto HLA-DR alel. Tento sdílený epitop má kladný náboj a podílí se na tvorbě vazebného místa na MHC glykoproteinech II. třídy. Zajímavé je, že MHC glykoproteiny II. třídy se záporně nabitým vazebným místem (například alela DRB1*0402) mohou chránit před rizikem propuknutí RA.
Další genetickou predispozicí zodpovědnou za náchylnost k RA by mohla být zvýšená schopnost citrulinovat peptidy, kterou mají na svědomí některé haplotypy lokusu peptidylarginin deiminázy 4 (PAD4) produkující velmi stabilní transkripty, které kódují enzym PAD4 zodpovědný za citrulinaci peptidů.

Environmentální rizikové faktory
Nejvýznamnější environmentální rizikový faktor představuje kouření tabáku, které zvyšuje riziko propuknutí séropozitivní RA. Také vystavení pasivnímu kouření v dětství zvyšuje riziko. Dalšími rizikovými faktory je nízký socioekonomický status a zvýšený index tělesné hmotnosti. Také týrání v dětství může mít vliv. Nebezpečné pro propuknutí séropozitivní RA je také vystavení oxidu křemičitému, ke kterému může dojít například na stavbách, ale převážně při vrtání hornin a drcení kamenů. Toto riziko dále roste, pokud člověk vystavený oxidu křemičitému je kuřák.
Nicméně bylo zjištěno, že pravidelné a umírněné pití alkoholu může představovat účinnou prevenci proti propuknutí RA a u pacientů, u kterých RA již propukla, snižuje závažnost tohoto onemocnění.
Etiologie
Původní příčina, která u konkrétního člověka vyvolá rozvoj nemoci, není dosud známa.
Propuknutí autoimunitní reakce může mít na svědomí bakterie Porphyromonas gingivalis, která se nachází v ústní dutině a způsobuje parodontózu. Tato bakterie citrulinuje proteiny, například fibrinogen a α-enolázu, ovšem na rozdíl od lidských PAD enzymů musí nejprve dojít k proteolytickému rozštěpení proteinu. Tento rozdílný mechanismus citrulinace bakteriálními PAD enzymy může tedy pravděpodobně zapříčinit porušení tolerance vůči těmto peptidům a způsobit vznik epitopů, vůči kterým neexistuje imunologická tolerance.
V posledních letech se diskutuje i role střevního mikrobiomu na patogenezi řady imunitně zprostředkovaných onemocnění, včetně RA.
Imunopatogeneze
Revmatoidní artritida patří do skupiny autoimunitních onemocnění, což znamená, že její základní příčina tkví v porušeném imunitním systému. Ten reaguje proti tkáním vlastního těla a poškozuje je tím, že v nich vyvolává chronický zánět. Z kloubů jsou nejčastěji postižena zápěstí a drobné klouby na rukou a na nohou.
U kloubu dochází k poškození ve dvou úrovních. Nejprve u časné formy RA dojde vlivem zánětu ke ztluštění synoviální membrány a vylučování tekutiny do kloubu. Synovitida neboli zánět synoviální membrány se typicky projevuje bolestí, otokem a ztuhlostí kloubů a vede ke snížené pohyblivosti. Pokud není léčena, vede k destrukci kloubu, která je patrná na rentgenových snímcích jako erozivní poškození v místech úponu synoviální membrány ke kosti a případné zúžení kloubní štěrbiny
Buňky zapojené do imunopatogeneze
Synoviální membrána je za normálních okolností tenká a obsahuje relativně malý počet buněk, ale vlivem infiltrace imunitních a efektorových buněk během zánětu se stává hyperplastickou. Uvnitř postiženého kloubu dochází ke vzájemným interakcím mnoha druhů imunokompetentních buněk a produkci cytokinů. Cytokiny zapojené do progrese poškození kloubů jsou například IL-1β, TNF-αa IL-17. Synoviální tekutina pacientů s časnou a etablovanou formou RA obsahuje odlišné spektrum cytokinů. Například TNF-α hraje roli při časné formě RA, kdežto IL-1β v průběhu etablované RA.
V synovii se mohou tvořit folikuly tvořené B a T lymfocyty a folikulárními dendritickými buňkami. Tyto folikuly mohou také přes lymfotoxin-β interagovat s fibroblasty a vést tak k produkci proteáz (např. matrixové metaloproteinázy) a dalších prozánětlivých mediátorů. Výsledkem je destruktivní zánětlivé prostředí v kloubu, které má schopnost se samo udržovat.
Trombocyty produkují prozánětlivý prostacyklin a uvolňují prozánětlivé mikročástice, které interagují s leukocyty a vedou ke vzniku systémového zánětu.
Neutrofilní granulocyty jsou v synoviální tekutině aktivovány revmatoidním faktorem a autoprotilátkami proti citrulinovaným peptidům, což vede k jejich degranulaci, uvolnění reaktivních forem kyslíku (ROS), kyseliny chlorné a proteáz. Toto vede k degradaci hyaluronové kyseliny a aktivaci cytokinů. Citrulinované peptidy, proti kterým se tvoří autoprotilátky, jsou dokonce neutrofilními granulocyty produkovány mechanismem nazývaným neutrofilní extracelulární past (NETóza).
Imunokomplexy
Na vzniku synovitidy se podílí cirkulující imunokomplexy, což jsou komplexy antigenu s protilátkami.
Vysoké koncentrace autoprotilátek proti citrulinovaným peptidům (ACPA) a revmatoidního faktoru (RF) jsou spojeny s vážnějším průběhem nemoci a nižší pravděpodobností dosažení remise. Díky účinné léčbě může někdy dojít k poklesu koncentrace RF a ACPA, není to ovšem pravidlem. Koncentrace RF klesá rychleji, více a u většího počtu pacientů s RA než koncentrace ACPA. Někteří pacienti se tedy mohou stát RF-negativní, ale ojediněle se stanou ACPA‑negativní.
Autoprotilátky proti citrulinovaným peptidům
U séro-pozitivních pacientů se v séru nachází autoprotilátky proti citrulinovaným peptidům produkované plazmatickými buňkami. Jde především o imunokomplexy IgG a IgM. Citrulinované peptidy vznikají posttranslační modifikací, kdy je aminokyselina argininpřeměněna na citrulin. K této modifikaci dochází deiminací pomocí enzymu PAD. Citrulinované peptidy pravděpodobně aktivují Th lymfocyty tím, že se ve velké míře vážou na MHC glykoproteiny II. třídy se sdíleným epitopem. Tato jejich zvýšená schopnost vázat se na MHC molekuly je pravděpodobně způsobena tím, že modifikací argininu na citrulin dochází ke změně náboje, kdy je nabitá skupina zaměněna za nenabitou skupinu, která má lepší schopnost vázat se do vazebného místa těchto MHC molekul.
Séro-pozitivní pacienti mají závažnější průběh nemoci a poškození kloubů než séro-negativní pacienti. Autoprotilátky proti citrulinovaným peptidům se nachází až u 70 % pacientů s časnou formou RA.
Revmatoidní faktor
Revmatoidní faktor je autoprotilátka proti Fc části imunoglobulinu G (IgG) a je výsledkem polyklonální aktivace B lymfocytů. Revmatoidní faktor tvoří imunokomplexy, které se nachází v séru a synoviální tekutině, a jejich přítomnost u jedinců, u kterých nebyla zatím diagnostikována RA, je považována za rizikový faktor k propuknutí této nemoci.
Příznaky

- prodromální (předchází vlastním projevům choroby)
- subfebrilie
- hubnutí
- únava
- kloubní
- bolest (nejdříve drobných kloubů)
- ranní ztuhlost, zduření
- omezení pohyblivosti
- deformity kloubů a ankylozy
- kůže na prstech je lesklá, hladká, atrofická
- mimokloubní
- oční příznaky (záněty skléry)
- nervové poškození
- anemie
Diagnostika
Aby se zastavila progrese této nemoci a nedocházelo dále k nevratnému poškození kloubů, je zcela zásadní včasná diagnóza a zahájení léčby během co nejkratší doby od nástupu prvních symptomů. Pro diagnostiku RA se využívá stanovení revmatoidního faktoru (RF) a protilátek proti citrulinovaným proteinům (ACPA). Tyto cirkulující autoprotilátky mohou být detekovány už 9 let před propuknutím klinických příznaků RA.
Podle doporučení z roku 2010 od Americké revmatologické asociace a Evropské ligy proti revmatismu by měli být jedinci vyšetřeni, zda u nich nepropukla RA, pokud mají synovitidu přítomnou alespoň v jednom kloubu, kterou nelze lépe vysvětlit pomocí jiné diagnózy. RA je definována dosažením skóre 6 a výše z 10. Do výpočtu tohoto skóre se zahrnuje počet a typ oteklých a citlivých kloubů, délka trvání symptomů, alespoň jeden sérologický test (RF nebo ACPA) a jeden test na reaktanty akutní fáze, což je sedimentace erytrocytů, nebo C-reaktivní protein (CRP).
Pro správnou diagnostiku a léčbu RA jsou nejdůležitější následující vyšetření:
- Odběr a vyšetření krve – při odběru krve se odebírá pouze obvyklé malé množství. Z několika mililitrů je možno získat informace o průběhu a aktivitě choroby. Důležité je především vyšetření revmatoidního faktoru, což je druh autoprotilátky, který se vyskytuje až u 80 % pacientů s revmatoidní artritidou. Z krve je rovněž možno určit stupeň zánětlivé aktivity, především podle počtu bílých krvinek a koncentrace CRP.
- Rentgenové vyšetření – rentgenové snímky se pořizují pravidelně v průběhu nemoci. Pro lékaře je důležitá možnost srovnat rentgenové snímky z různých časových období a určit tak, zda a jak rychle postupuje zánětlivý proces poškozující klouby.
- Punkce kloubu – některé postižené klouby jsou zvětšené a bolestivé nejen kvůli otoku okolních tkání, ale také kvůli vyššímu množství nitrokloubní tekutiny, která je vylučována do kloubní dutiny. V takových případech se často provádí kloubní punkce – nabodnutí kloubu dlouhou jehlou a nasátí zmnožené nitrokloubní tekutiny. Punkce se provádí u větších kloubů, jako je koleno, kyčel nebo zápěstí. Z nasáté tekutiny je možné zjistit pravděpodobnou příčinu zánětu, a odsátí určitého množství tekutiny rovněž uleví postiženému kloubu a zmírní bolest.
Možnosti léčby
Možnosti léčby RA dělíme na nefarmakologické, farmakologické a chirurgické. RA je prozatím nevyléčitelné onemocnění, proto je cílem léčby dosažení remise nebo nízké aktivity nemoci. Čím déle se po diagnóze otálí se zahájením léčby, tím horších výsledků je během terapie dosaženo. Dochází k nevratnému poškození kloubů a je menší šance dosáhnout remise. Z tohoto důvodu je zcela zásadní zahájit léčbu co nejdříve se stanovením diagnózy.
Nefarmakologické
Tento typ léčby je založen na pravidelném cvičení, jehož cílem je posílit svaly, zachovat maximum pohybu kloubu a jeho funkčnost.
Chirurgické
V pokročilých stadiích revmatoidní artritidy lze chirurgicky odstranit zničené klouby a nahradit je umělými implantáty (takzvanými endoprotézami). Implantát, který obnovuje funkci zničeného kloubu, je možné použít jako náhradu u kloubů kyčelních, kolenních, ramenních, loketních, zápěstních i prstových. Chirurgická léčba pacienta také zbaví bolestí v postiženém kloubu.
Farmakologické
K léčbě RA lze v dnešní době vybírat z široké palety dostupných léků patřících do různých kategorií. Základem terapie jsou chorobu modifikující antirevmatické léky (anglicky disease-modifying antirheumatic drugs, DMARD), které zmírňují zánět a redukují progresi strukturálního poškození. Dělí se do několika kategorií, viz tabulka č.1. Dalším typem léků užívaných při terapii RA jsou nesteroidní protizánětlivé léky (anglicky nonsteroidal anti-inflammatory drugs, NSAID), které jsou ovšem pouze symptomatické. Snižují tedy bolest, ztuhlost a zlepšují pohyblivost kloubů, ale nechrání je před poškozením. S jejich dlouhodobým používáním je také spojena nezanedbatelná kardiovaskulární a gastrointestinální toxicita. Takže by měly být NSAID podávány po kratší dobu a v nízkých dávkách. Dále se užívají také glukokortikoidy, které mají rychlý a výrazný protizánětlivý účinek. Navíc mohou zabránit destrukci kloubů a významně zmírňují příznaky onemocnění. Nicméně při dlouhodobém užívání mají závažné vedlejší nežádoucí účinky (např. osteoporóza, infekce, gastrointestinální krvácení nebo žaludeční vředy). Glukokortikoidy se doporučuje podávat jako součást iniciální léčebné strategie v případě aktivního onemocnění nebo u etablované RA při relapsu onemocnění. Dávku je nutné postupně snižovat až k vysazení, ideálně do 3 měsíců, maximálně však do 6 měsíců. Tabulka č.1: Schválené chorobu modifikující antirevmatické léky pro léčbu RA a jejich rozdělení do kategorií.
| 1. sDMARD | |
| – csDMARD | methotrexát, sulfasalazin, leflunomid, hydroxychlorochin, chlorochin a soli zlata |
| – tsDMARD | baricitinib a tofacitinib |
| 2. bDMARD | |
| – boDMARD | adalimumab, certolizumab pegol, etanercept, golimumab, infliximab, anakinra, sarilumab, tocilizumab, abatacept a rituximab |
| – bsDMARD | odvozené od adalimumabu, etanerceptu, infliximabu a rituximabu |
Vysvětlení použitých zkratek: Syntetické DMARD (anglicky synthetic DMARD, sDMARD), konvenční syntetické DMARD (anglicky conventional synthetic DMARD, csDMARD), cílené syntetické DMARD (anglicky targeted synthetic DMARD, tsDMARD), biologické DMARD (anglicky biological DMARD, bDMARD), biologické originální DMARD (anglicky biological original DMARD, boDMARD) a biosimilární DMARD (anglicky biosimilar DMARD, bsDMARD).
Methotrexát
Methotrexát je nejčastěji předepisovaný lék, který navíc příznivě ovlivňuje mortalitu způsobenou RA. Bylo zjištěno, že snižuje úmrtnost na kardiovaskulární onemocnění. Pokud není přítomna žádná kontraindikace, je doporučováno začít léčbu methotrexátem, obvykle spolu s užíváním glukokortikoidů, jejichž dávka se musí postupně snižovat až k vysazení. Doporučená dávka methotrexátu je 25–30 mg týdně spolu s užíváním kyseliny listové, která snižuje riziko kardiovaskulárních onemocnění. Po dosažení cíle léčby (obvykle do 6 měsíců od začátku terapie) lze zkusit dávku methotrexátu snížit. Pokud ovšem nedojde ke zlepšení do 3 měsíců od zahájení léčby, lze methotrexát buď kombinovat s jiným csDMARD (leflunomid, sulfasalazin), nebo jej zcela nahradit. V případě přítomnosti nepříznivých prognostických ukazatelů (vysoká aktivita nemoci, pozitivní autoprotilátky a časné erozivní poškození kloubů) by měla být indikována biologická léčba.
Biologická léčba
Terapie těmito léky se zahajuje po selhání léčby pomocí csDMARD. Je doporučeno je kombinovat s methotrexátem nebo jiným csDMARD. Po dosažení cíle léčby lze snížit dávku nebo zvýšit interval podávání biologického léku. Nicméně u některých pacientů není ani tato léčba účinná, případně může dojít k postupnému vymizení účinnosti, nebo je doprovázena nežádoucími vedlejšími účinky. V těchto případech lze podat jiný biologický lék, případně zahájit léčbu inhibitorem JAK. Problém během této terapie představuje tvorba protilátek proti těmto biologickým lékům, které mají pravděpodobně na svědomí snížení účinnosti terapie a některé vedlejší účinky. Tvorbu těchto protilátek snižuje současné užívání methotrexátu.
Inhibitory TNF
Prozatím schválené léky jsou uvedeny níže. Přestože všechny neutralizuji TNF-α, což je cytokin důležitý v patogenezi RA, nejsou identické, protože se odlišují svou molekulární strukturou.
- adalimumab (Humira) – Monoklonální IgG1 protilátka proti TNF-α.
- certolizumab pegol – Fab fragment protilátky konjugovaný s molekulou polyethylenglykolu.
- etanercept – Fúzní protein receptoru pro TNF a Fc části IgG1.
- golimumab – Monoklonální protilátka proti TNF-α.
- infliximab (Remicade) – Chimérická monoklonální IgG1 protilátka proti TNF-α.
Inhibitory receptoru pro IL-6
- tocilizumab (Actemra)
Humanizovaná monoklonální IgG1 protilátka proti receptoru pro IL-6, která se užívá pro léčbu středně těžké až těžké formy RA, a to u dospělých, u kterých selhala předchozí léčba inhibitory TNF.
- sarilumab (Kevzara)
Monoklonální IgG1 protilátka blokující jak rozpustný, tak transmembránový receptor pro IL-6.
Blokátory kostimulace T lymfocytů
- Abatacept
Abatacept je rozpustný rekombinantní fúzní protein, který se skládá z extracelulární domény lidského cytotoxického T-lymfocytárního antigenu (CTLA-4) a Fc části lidského IgG1. Snižuje aktivitu imunitního systému tím, že blokuje kostimulační děje mezi imunokompetentními buňkami, konkrétně mezi APC a T lymfocyty, a tím zabraňuje aktivaci a proliferaci T lymfocytů a rozvoji imunitní reakce. Do kostimulace jsou zapojeny CD80/CD86 na APC a CD28 na T lymfocytech. Abatacept se váže na CD80/CD86 na APC, čímž zabraňuje kostimulaci T lymfocytů, a tedy jejich aktivaci. Také ovlivňuje expresi adhezivních molekul na monocytech, čímž snižuje jejich migraci do synovie a zvyšuje tedy jejich množství v krvi. T lymfocyty mají díky abataceptu sníženou schopnost produkovat prozánětlivé cytokiny jako IL-17 a IFNγ.
Depleční terapie proti B lymfocytům
- rituximab
Rituximab je chimérická monoklonální protilátka vyrobená pomocí genetického inženýrství, jejíž jedna část je myší a druhá lidská. Váže CD20 na povrchu B lymfocytů. CD20 je ideální cíl pro depleční terapii, protože je exprimován na povrchu B lymfocytů, ale ne na povrchu kmenových a plazmatických buněk, takže hladiny IgG, IgM a IgA zůstanou v normálním rozmezí. Rituximab redukuje počet B lymfocytů jejich lýzou na základě cytotoxicity závislé na komplementu, na základě cytotoxicity buněčně zprostředkované, nebo na základě signálem zprostředkované apoptózy.
„Biosimilární“ léky
Protože jsou biologické léky velmi drahé, ne všichni pacienti mohou tuto terapii podstoupit. Pro řadu z nich představují naději tzv. biosimilární léky, které jsou odvozeny od původních biologických léků, což je umožněno vypršením jejich patentu. Jelikož mají biologické léky poměrně složitou strukturu a jsou vytvářeny živými organismy, jejich jednotlivé vyrobené várky se mohou lišit. Proto není možné vytvořit naprosto identické molekuly nebo generické léky. Prozatím byly v Evropské unii a jiných zemích schváleny biosimilární léky adalimumabu, etanerceptu, infliximabu a rituximabu a další (jako například odvozené od golimumabu a certolizumabu pegol) jsou ve vývoji.
Inhibitory JAK kináz
Inhibitory JAK kináz jsou malé cílené syntetické léky, které mohou vstoupit do buňky a regulovat v ní intracelulární přenosy signálu. Patří k nim baricitinib a tofacitinib
- Baricitinib (komerční název Olumiant)
Baricitinib je selektivní inhibitor JAK1 a JAK2. Kromě léčby RA se v klinických studiích zkoumá i při léčbě psoriázy. V únoru 2017 byl schválen v Evropské unii pod názvem Olumiant pro léčbu RA buď jako monoterapie, nebo v kombinaci s methotrexátem.
- Tofacitinib (komerční název Xeljanz)
Tofacitinib na rozdíl od baricitinibu inhibuje JAK3. Stejně jako baricitinib je podáván perorálně, zasahuje do buněčné signalizace a narušuje tak účinek několika cytokinů. Tofacitinib byl původně vytvořen za účelem využití k imunosupresi při transplantacích orgánů. Tento lék je v současnosti také zkoumám v klinických studiích při léčbě psoriázy. V březnu 2017 byl pod komerčním názvem Xeljanz schválen i v Evropské unii pro léčbu RA.
Výzkum nových léků
I přes pokrok v léčbě zavedením biologických a cílených syntetických léků během posledních let stále řada pacientů nevykazuje dostatečnou odpověď na tyto terapie, nebo je postihnou závažné vedlejší účinky. Z těchto důvodu je stále třeba vyvíjet nové léky, z nichž jsou některé uvedeny níže.
Hybridy nesteroidních protizánětlivých léků a inhibitorů karbonické anhydrázy
Tyto hybridy, hlavně tedy hybrid s ibuprofenem, zatím ukázaly na krysím modelu svůj potenciál zmírňovat příznaky RA, například bolest.
Decernotinib
Selektivní inhibitor JAK3, který je současně zkoumám v klinických studiích.
Filgotinib
Selektivní JAK1 inhibitor testován v klinických studií kromě RA také při léčbě Crohnovy choroby.
Clazakizumab
Je to humanizovaná monoklonální protilátka, která je podávána subkutánně a váže cirkulující cytokin IL-6.
Olokizumab
Olokizumab je humanizovaná monoklonální protilátka, která váže cytokin IL-6 a tím snižuje jeho hladinu v krvi.
Mavrilimumab
Mavrilimumab je monoklonální protilátka, která blokuje receptor pro GM-CSF. Je podáván subkutánně a je to první biologický lék, který byl klinicky testován za účelem inhibice této dráhy. V prozatím provedených klinických studiích ukázal slibné výsledky při snížení aktivity RA, nicméně je třeba provést studie další a jeho účinek potvrdit.
MOR103
MOR103 je monoklonální protilátka proti GM-CSF (neváže receptor pro GM-CSF jako mavrilumab, ale váže přímo GM-CSF).
Bispecifické protilátky
Další novou slibnou možností léčby jsou bispecifické protilátky, které představují možnost inhibice 2 signálních drah pomocí jedné molekuly. Tato metoda by mohla být přínosná pro pacienty, kterým dostatečně nezabrala léčba, která inhibovala jeden cytokin, nebo u kterých postupem času došlo ke snížení účinnosti této léčby.
Příkladem je bispecifická protilátka, která inhibuje IL-17 a TNF-α. Je založena na zjištění, že kombinovaná inhibice IL-17 a TNF-α je účinnější, má protizánětlivý účinek a obnovuje hemostázu kostí, která je narušena při RA.
Další zkoumaná bispecifická protilátka inhibuje IL-1β a IL-17A. Prozatím prokázala schopnost zabraňovat destrukci chrupavky u myší a také dokázala zabránit rozšíření Th17 lymfocytů. U synoviálních fibroblastů prokázala schopnost snížit produkci IL-6.
Lázně
Lázeňská léčba revmatoidní artritidy je vhodná především pro ty pacienty, u nichž nemoc není příliš aktivní. Při některých formách lázeňské léčby může totiž dojít i k oživení zánětu, zejména jsou-li používány příliš teplé procedury. O vhodnosti lázeňské léčby může rozhodnout pouze lékař-revmatolog, který také nese odpovědnost za to, že pobyt v lázních nezhorší průběh nemoci. Obecně je lázeňský pobyt možné předepsat pacientům od II. stupně choroby s funkčním postižením typu b.
Na doporučení lékaře pacient většinou absolvuje pobyt v průměrném rozsahu jeden měsíc až jeden a půl měsíce. Lázeňský pobyt by měl přinášet zintenzivnění celkové léčby. Prospěšná je možnost celodenního rozvržení léčby a často i příznivé působení příjemného lázeňského prostředí. Při vzniku aktuálních problémů bývá navíc k dispozici odborná lékařská pomoc.
Pojem naleznete v následujících článcích:
-
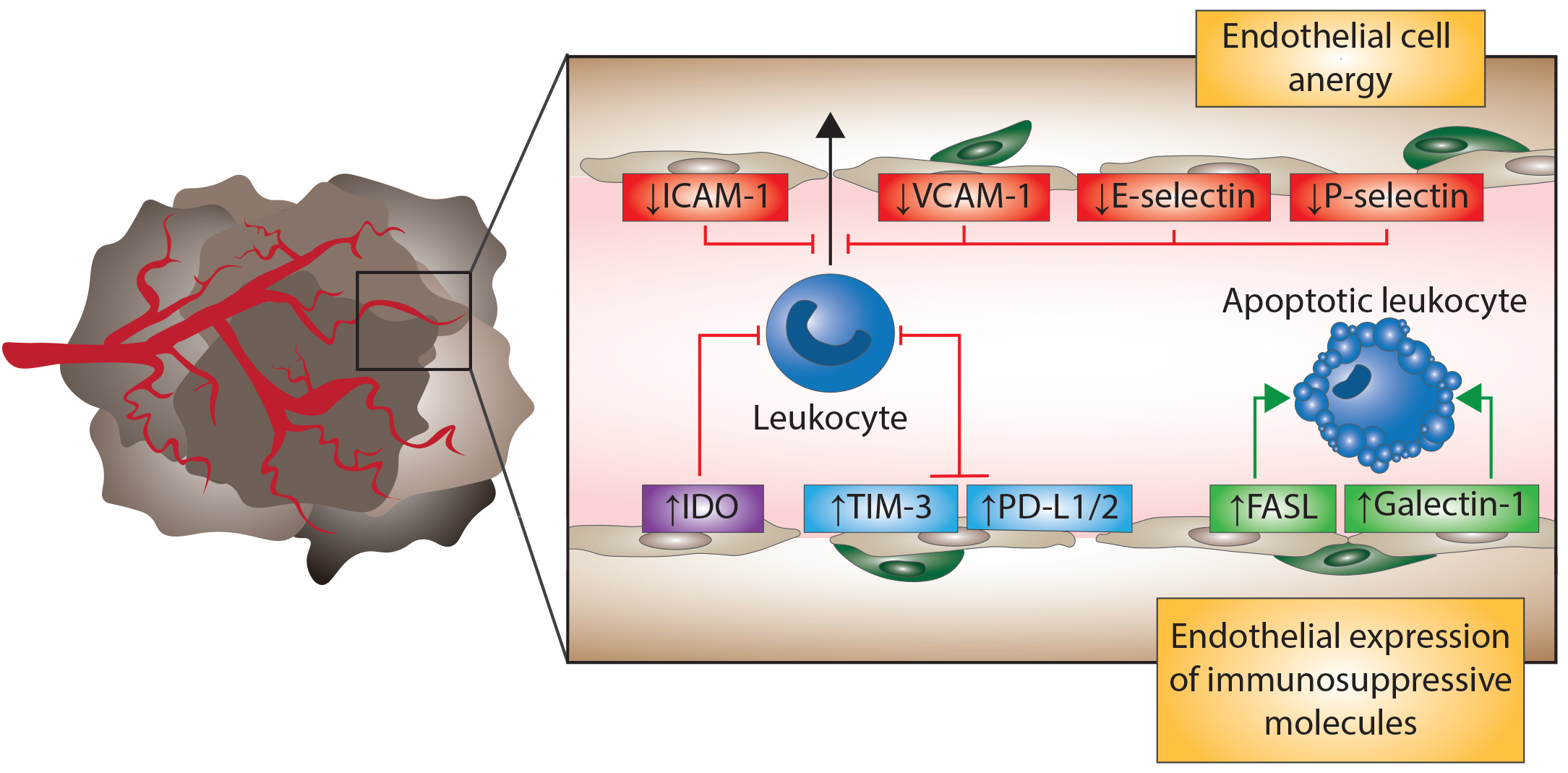
Anergie
Anergie je imunologický pojem, který popisuje neschopnost reakce lidského imunitního systému proti cizí látce zapříčiněnou přímou indukcí tolerance v periferních lymfocytech. Imunitní systém je v případě anergie neschopný…
-
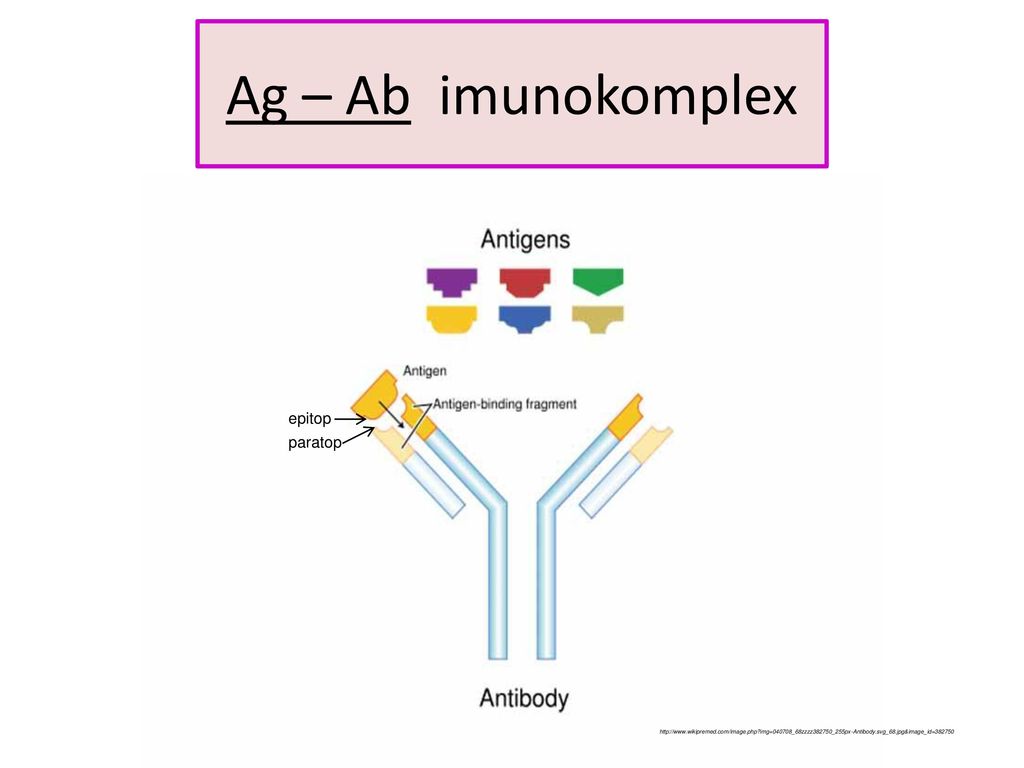
Imunokomplex
Imunokomplex je komplexní molekula vzniklá navázáním protilátky na antigen, respektive na jeho specifický epitop, event. v kombinaci s komplementovými fragmenty. Navázáním protilátky na antigen, tedy vznikem imunokomplexu, dochází…
-
Imunitní tolerance
Uvnitř brzlíku prochází důkladnou kontrolou T-lymfocyty; prochází pozitivní a negativní selekcí Imunitní tolerance je stav neodpovídavosti imunitního systému na určitý antigen nebo antigeny, např. látky a tkáně organismu.…
-
Autoprotilátka
Autoprotilátky jsou protilátky (imunoglobuliny) namířené proti antigenům vlastního organismu. Antigenem mohou být proteiny, glykoproteiny, nukleové kyseliny, fosfolipidy a glykofosfolipidy. Autoprotilátky se dělí na orgánově specifické a orgánově nespecifické.…
-
Dendritická buňka
Dendritické buňky (DC, z angl. Dendritic cells) tvoří spojnici mezi přirozenými a adaptivními mechanismy imunitního systému a jsou profesionálními buňkami prezentujícími antigeny. Představují různorodou skupinu buněk, které se…
-
Autoimunita
Autoimunitní choroby mohou postihovat různé systémy a orgány lidského těla Autoimunita je stav, při kterém některá ze složek imunitního systému reaguje na struktury vlastního organismu, které tím zpravidla…
-
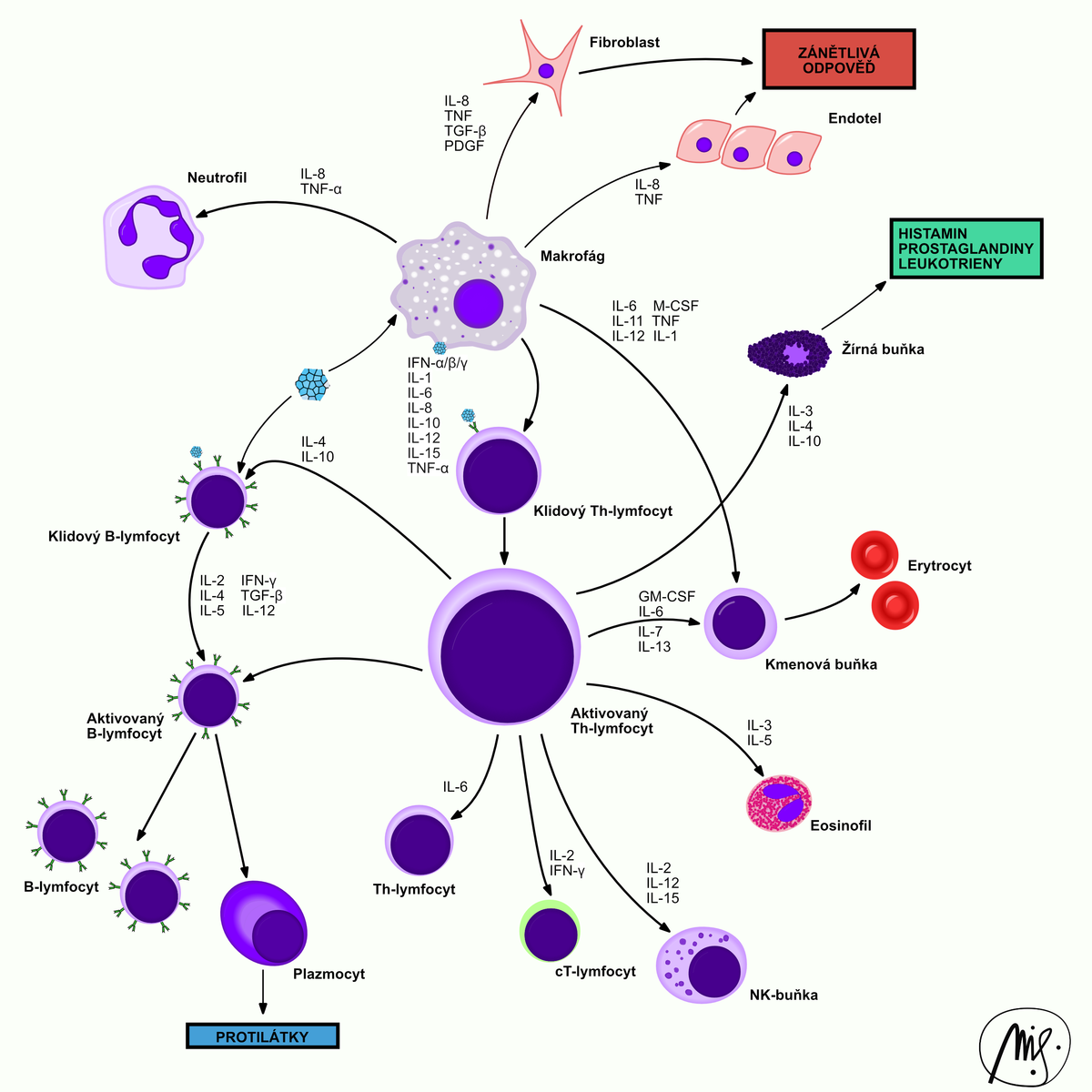
Pomocné T-lymfocyty
Pomocné T lymfocyty (Th lymfocyty, Th buňky), známé také jako CD4 buňky, jsou typem T lymfocytů, které mají důležitou roli v imunitním systému, konkrétně v adaptivním imunitním systému.…