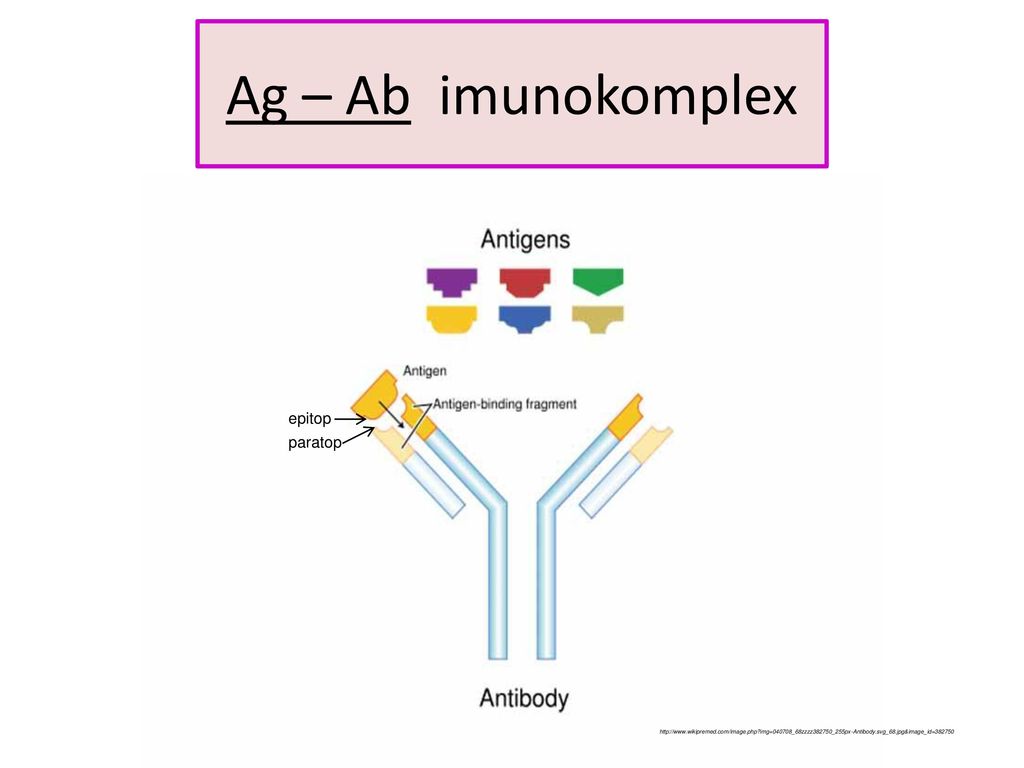
Imunokomplex je komplexní molekula vzniklá navázáním protilátky na antigen, respektive na jeho specifický epitop, event. v kombinaci s komplementovými fragmenty. Navázáním protilátky na antigen, tedy vznikem imunokomplexu, dochází k opsonizaciantigenu, jenž se tímto stává výrazně atraktivnější pro fagocytující buňky. Navázáním protilátky na antigen dochází k aktivaci komplementové kaskády klasickou cestou – navázáním proteinu C1 dochází k jeho aktivaci, čímž je zahájeno štěpení proteinů C4 a C2, kdy membránový komplex C4bC2a působí jako klasická C3 konvertáza; fragmenty C4a, C2b a C3a působí chemotakticky, fragment C3b má opsonizační účinky. Dále je průběh již shodný s alternativní cestou – k C3 konvertáze se připojí fragment C3b, tedy v případě klasické cesty C4bC2aC3b, kdy vzniká klasická C5 konvertáza, jejímž působením vzniká rozpustný C5a se silným chemotaktickým účinkem a dále C5b vytvářející s dalšími komplementovými proteiny (C6, C7, C8 a C9) lytický komplex.
Biologické účinky imunokomplexů
Poměr mezi množstvím antigenu a protilátky určuje velikost a tvar imunokomplexu, což má zásadní vliv na jeho další osud stejně jako izotyp zúčastněné protilátky – např. IgG3 a IgG1 dobře aktivují komplement na rozdíl třeba od IgG4 či IgA, které komplementneaktivují vůbec, což by v opačném případě u posledně zmíněného izotypu vedlo k poškození sliznic, kde právě IgA hraje hlavní roli v humorální části adaptivní imunity.
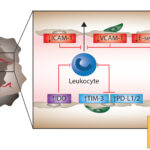
Řada buněk vrozené imunity disponuje na svém povrchu Fc receptorem (FcR) schopným vázat Fc konec imunoglobulinů. Většina FcR má slabou afinitu vůči jednotlivé molekule imunoglobulinu. Dojde-li však ke kontaktu FcR s imunokomplexem, jehož součástí je větší množství polyklonálních protilátek, dochází díky zesíťování k silnější stimulaci FcR, která již je schopna iniciovat intracelulární signalizační kaskádu. Imunokomplexy tedy zvyšují aviditu (empirický pojem vyjadřující sílu interakce polyvalentní protilátky s polyvalentním antigenem; avidita roste s afinitou jednotlivých interakcí protilátka – antigen) uvedené vazby.
Imunokomplex, a nikoli antigen samotný, je nutný k aktivaci dendritických buněk a makrofágů. Díky širokému spektru vlastností imunokomplexů daných právě proměnlivým poměrem mezi množstvím antigenu a protilátky a izotypem zúčastněné protilátky, jak zmíněno výše, je zajištěna správná aktivace různých typů fagocytů disponujících odlišnými kombinacemi povrchových FcR.
Regulace produkce protilátek
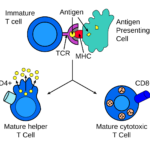
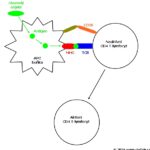
Imunokomplexy hrají roli v regulaci tvorby imunoglobulinů. B lymfocyty mají na svém povrchu navázané B receptory (BCR, což jsou povrchově vázané imunoglobuliny), které po rozeznání antigenu v nativní podobě (na rozdíl od T lymfocytů, které jsou schopny rozeznat pouze antigen prezentovaný v rámci povrchových MHC molekul) zahájí aktivaci buňky spočívající v diferenciaci v plazmatickou buňku produkující imunoglobuliny. Tato základní interakce může být imunokomplexem ovlivněna pozitivně i negativně:
- Je-li součástí imunokomplexu opsonizující komplementový fragment C3dg, dochází po jeho navázání na specifický komplementový receptor CR2 (CD21, který tvoří s CD19 heterodimer) k posílení interakce BCR – antigen.
- Vedle BCR je na povrchu B lymfocytů ještě přítomen FcγRIIb, který po vazbě s imunokomplexem, respektive s Fc částí IgG, naopak blokuje aktivaci B lymfocytu, což může vést až k indukci apoptózy.
Imunokomplexy jako příčina patologických stavů
Imunokomplexy mohou samy o sobě, dojde-li namísto jejich eliminace fagocyty naopak k jejich usazování neboli depozici v určitých orgánech, být příčinou některých patologických stavů, kdy mechanismem poškození tkání je aktivace fagocytů vazbou na FcR nebo aktivace komplementové kaskády s následnou chemotaxí neutrofilů. Usazování imunokomplexů je patofyziologickou příčinou vzniku imunopatologické reakce III. typu podle klasické klasifikace dle Coombse a Gella.
K rozvoji uvedené reakce může dojít i po jednorázovém setkání s antigenem. Jelikož podmínkou vzniku imunokomplexů je dostatečné množství protilátek, vznikají reakce většinou až s odstupem 10-14 dní od expozice antigenu. Za fyziologických okolností se setkáváme s časově omezenou imunokomplexovou reakcí např. při eliminaci infekčních agens, kdy se tvorba imunokomplexů může projevit třeba bolestmi svalů či kloubů. Je-li však antigen přítomen ve výrazném nadbytku nebo jedná-li se o tělu vlastní antigen, reakce probíhá s větší intenzitou či perzistuje a je pak označována za imunopatologickou.
Učebnicovým příkladem imunopatologické reakce III. typu s tvorbou imunukomplexů je tzv. sérová nemoc, která může vzniknout po podání xenogenního séra, tedy séra jiného živočišného druhu – např. reakce po podání koňského séra proti hadímu jedu, která může být paradoxně závažnější než účinek jedu samotného. Ze stejného důvodu není prakticky možné testovat lidské terapeutické monoklonální protilátky na modelových zvířatech, protože aplikace xenogenního imunoglobulinu vyvolá u zvířete tvorbu neutralizujících protilátek zkreslujících původní biologický účinek testované molekuly.
Dochází-li k vazbě protilátek na tělu vlastní antigeny – tzv. autoantigeny, hovoříme o tzv. autoimunitních onemocněních, při nichž je narušena autotolerance coby jednoho ze tří základních atributů imunitního systému (těmi zbylými dvěma jsou obranyschopnost a imunitní dohled). Příkladem takových onemocnění vzniklých na podkladě ukládání imunokomplexů mohou být lupus erythematodes či revmatoidní artritida.
Využití imunokomplexů v laboratoři
V in vitro prostředí se imunokomplexy vytvářejí pouze za ideálních podmínek. Na tvorbě imunokomplexů je založen princip imunochemických metod, přičemž příkladem jedné z nich, důležité spíše z historického hlediska, může být v soudním lékařství užívaná Uhlenhuthova metoda, při níž po navázání protilátek dochází k vysrážení specifických sérových proteinů (polyvalentní antigen) v podobě tzv. precipitátů (reakce bývá též nazývána jako precipitinová; precipitiny jsou protilátky schopné tvořit sraženiny neboli precipitáty), na základě čehož lze mezi sebou rozeznat vzorky krve od různých živočišných druhů.