Žírné buňky (též mastocyty) jsou efektorové buňky imunitního systému, známé pro svoji roli v patofyziologii alergické reakce. Vyvíjí se z myeloidní řady, svojí morfologickou stavbou se řadí mezi granulocyty. Žírné buňky byly objeveny v roce 1877 Paulem Ehrlichem v rámci jeho doktorské práce.
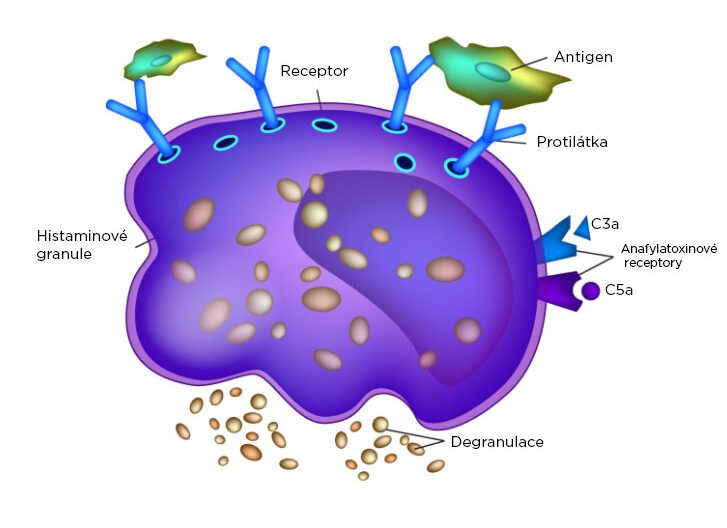
Granula žírných buněk obsahují histamin, řadu zánětlivých mediátorů, proteoglykany (heparin, chondroitinsulfát) a hydrolytické enzymy (zejména tryptázu). Při aktivaci žírných buněk dojde k vylití obsahu těchto granul (tzv. degranulace žírných buněk), což vede k lokální zánětlivé odpovědi. Existuje řada mechanismů, které vedou k aktivací žírných buněk. Nejvýznamnější z nich je přes navázání antigenu na IgE protilátky na povrchu žírných buněk. Tento mechanismus je také zodpovědný za alergickou reakci při expozici jinak neškodným antigenům (pyl, některá jídla). Spolu s bazofilními granulocyty se žírné buňky také podílí na patogenezi anafylaktického šoku. Mimo to se ale žírné buňky účastní celé řady fyziologických procesů, jako je hojení ran, oprava tkání, regulace zánětlivé odpovědi, udržování homeostázy střevních bakterií nebo udržování funkce sliznic.
Struktura a lokalizace buněk
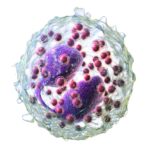
Žírné buňky se svojí morfologickou stavbou řadí mezi granulocyty. Oproti bazofilům, které mají členité jádro, mají mastocyty jádro spíše kulaté. Granula žírných buněk se barví Bismarckovou hnědí, mukopolysacharidy a glykosaminoglykany toludinovou modří.
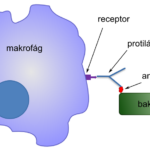
Žírné buňky mají na celém svém povrchu vystavené Fc receptory, na které se velmi pevně vážou IgE protilátky. Ty tak pokrývají celý povrch mastocytu. Navázání antigenu na tyto IgE protilátky představuje hlavní cestu aktivace žírných buněk.
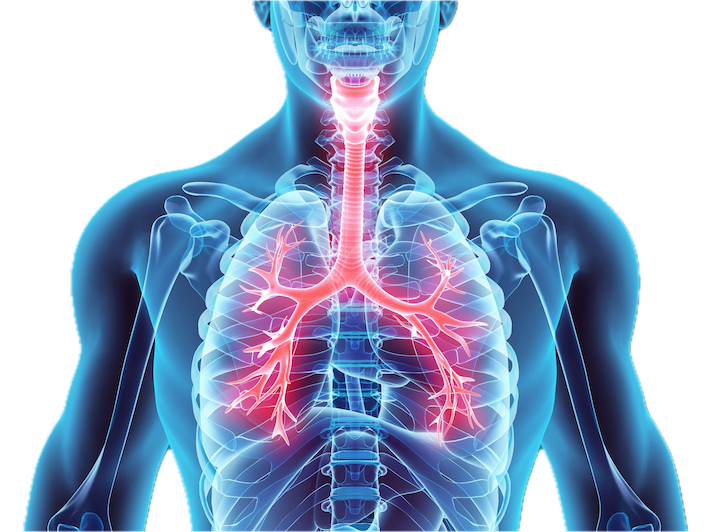
Žírné buňky se nachází ve všech vaskularizovaných tkáních s výjimkou centrálního nervového systému a sítnice, zejména pak v místech možného vniku patogenů na rozhraních mezi vnitřním a vnějším prostředím, tj. ve sliznici dýchacích cest, trávicího traktu, v kůži, ústech, spojivkách a v nosu. Dále se nachází v pojivové tkáni v okolí krevních a lymfatických cév a nervů. Podle jejich lokalizace, struktury a funkce lze mastocyty dělit na pojivové a slizniční.
Funkce
Žírné buňky mají na svém povrchu navázané IgE protilátky. Hlavní imunitní funkcí žírných buněk je obrana proti parazitárním infekcím, např. vyvoláním zvracení a průjmu v případě střevních parazitů nebo vyvoláním kašlání v případě plicních parazitů. V rozvinutých zemích jsou nicméně parazitární infekce spíše vzácné. Z tohoto důvodu funkce obrany proti parazitům ztrácí na důležitosti a žírné buňky se stávají významnými zejména pro svoji roli v patofyziologii alergické reakce 1. typu. U alergií B-buňky produkují IgE protilátky proti jinak neškodným antigenům (pyl, některé potraviny, léky, …). Ty jsou navázány na povrch žírných buněk a při expozici antigenu dochází k jejich aktivaci a ke spuštění imunitní odpovědi. Degranulaci žírných buněk ale mohou vyvolat i některé aminy a alkaloidy, např. morfin, kurare alkaloidy, antibiotika polymyxiny.
Při kontaktu antigenu s IgE protilátkami na mastocytu dojde k navázání antigenu na protilátky a k propojení (cross-linking) více IgE protilátek vazbou na antigen. To způsobí sdružení několika molekul receptoru a spuštění signalizační kaskády, která vede k aktivaci žírné buňky. Při aktivaci žírné buňky dojde k degranulaci, tj. k fúzi intracelulárních granulí s cytoplazmatickou membránou a k vylití obsahu granulí do okolí buňky. Působky obsažené v granulích žírných buněk mohou parazita buď poškozovat přímo nebo prostřednictvím vyvolání imunitní odpovědi a rozvojem dalších obranných mechanismů. Stejný mechanismus je u žírných buněk ale zodpovědný také za projevy časného typu přecitlivělosti (alergie) na neškodné antigeny.
Granula žírných buněk obsahují hydrolytické enzymy (serinové proteázy, zejména tryptázu), proteoglykany (heparin, chondroitinsulfát), histamin a serotonin a řadu cytokinů. Všechny z těchto látek jsou bioaktivní a multipotentní, kvůli čemuž dochází zároveň k ovlivnění velkého množství buněk a tkání (např. dendritických buněk, makrofágů, T-lymfocytů, B-lymfocytů, fibroblastů, endoteliálních buněk nebo buněk epitelu).
Fyziologie
Aktivace žírných buněk
Žírné buňky mají na celém svém povrchu Fc receptory pro IgE (FcεR1). Tyto receptory mají tetramerní strukturu a jsou tvořené jednou podjednotkou ɑ a β a dvěma podjednotkami ɣ. Na extracelulární část podjednotky ɑ se velmi silně vážou IgE protilátky. Díky tomu je celý povrch mastocytu pokrytý IgE protilátkami, které jsou schopné rozpoznávat příslušné antigeny. IgE protilátky syntetizují B-buňky v případě stimulace CD4+ Th2 buňkami. Podjednotka β obsahuje jeden immunoreceptor tyrosin-based activation motif (ITAM), každá podjednotka ɣ také obsahuje jeden ITAM.
Signalizační kaskáda vedoucí k degranulaci žírných buněk začíná fosforylací tyrozinů v ITAM na β a ɣ podjednotkách pomocí Lyn kinázy (patří do rodiny Src kináz). Na fosforylované ITAM se následně váže přes SH2 doménu Syk kináza (rodina Src kináz). Syk kináza následně fosofryluje další proteiny účastnící se signalizační kaskády, včetně fosfolipázy C. Ta produkuje inositoltrifosfát a diacylglycerol, které mají úlohu druhých poslů. Signalizační kaskáda končí u mobilizace vápníku z endoplazmatického retikula žírných buněk a degranulace. Zároveň dochází k translokaci faktoru NFκB do jádra a k produkci cytokinů, leukotrienu C4 a prostaglandinu PGD2.
Uplatňuje se i signalizační dráha začínající Fyn kinázou. Tato dráha je komplementární k dráze Lyn kinázy. Dochází k aktivaci mTOR a tím k produkci cytokinů.
Mimo Fc receptorů se na žírných buňkách nachází také „pattern recognition receptors“ rozpoznávající damage-associated molecular pattern (DAMP) a pathogen-associated molecular pattern (PAMP). Dále jsou přítomné toll-like receptory (TLR 1-7 a 9). Při aktivaci těchto receptorů dochází k uvonění zánětlivých mediátorů s cílem eliminovat patogen. Mechanismus eliminace se ale může lišit podle toho, jaké receptory byly aktivovány. V případě aktivace TLR4 receptorů pomocí lipopolysacharidu G- bakterií dochází pouze k produkci cytokinů bez degranulace žírných buněk. Naopak v případě aktivace TLR2 receptorů pomocí peptidoglykanů G+ bakterídochází jak k produkci cytokinů, tak k degranulaci žírných buněk.
Z dalších látek produkovaných žírnými buňkami lze zmínit TNF-ɑ, který způsobuje aktivaci fagocytů a zvýšení exprese adhezivních molekul na endoteliích); TNF-β, který se účastní procesů hojení ran; IL-5, který stimuluje eozinofily; a IL-6, který stimuluje B-buňky k produkci imunoglobulinů.
Migrace a diferenciace žírných buněk
Terminálně diferencované žírné buňky se nachází v epiteliálních tkáních na rozhraních mezi organismem a vnějším prostředím (např. v trávicím traktu nebo dýchacích cestách) a v pojivových tkáních okolo cév a hladké svaloviny. Prekurzory žírných buněk se z kostní dřeně uvolňují do krevního řečiště. Následně migrují do svých cílových tkání, kde teprve dozrávají a vyvíjejí se na terminálně diferencované žírné buňky. Migrace do tkání je determinována lokálním mikroprostředím, včetně adhezních molekul, chemokinů, cytokinů a růstových faktorů. Jednou z cílových tkání pro progenitory žírných buněk je sliznice tenkého střeva. Migrace je zahájena prostřednictvím interakcí mezi integriny ɑ4β7 a VCAM-1 na endotelu cév, čímž je umožněna extravazace progrenitorových buněk. Ty jsou dále směřovány do tenkého střeva pomocí CXCR2. Jiná situace je v případě dýchacích cest: za normálních fyziologických podmínek se v plicích nachází pouze malé množství progenitorů žírných buněk. Ty jsou do plic povolávány až v případě probíhajícího zánětu. Jejich migrace je opět zahájena prostřednictví interakcí ɑ4β7 integrinů s VCAM-1 na endotelu a dále je řízena prostřednictvím CXCR2, CCR-2 a CCL-2.
Klinický význam
- Ochrana před parazitární infekcí
- Alergie, anafylaxe
- Asthma
- Mastocytóza
- Mastocytomy
- Mast cell activation syndrom (MCAS)
Žírné buňky se nachází ve spodních vrstvách kůže. K jejich aktivaci může dojít buď po přímém kontaktu kůže s antigenem nebo při přenosu antigenu z gastrointestinálního traktu. Projevy aktivace žírných buněk v kůži zahrnují kopřivku (alergickou i autoimunitní), zarudnutí a angioedém.
Žírné buňky v dýchacích cestách mohou ovlivňovat jak epitel, tak hladkou svalovinu dýchacích cest. Při degranulaci žírných buněk dochází k otoku sliznice na podkladě zvýšení propustnosti krevních kapilár a může docházet ke konstrikci dýchacích cest. Zároveň dochází také ke zvýšení produkce hlenu a kašlání. Může docházet i ke kontrakci hladké svaloviny a při současné aktivaci bazofilních granulocytů až k bronchospasmu.
Žírné buňky hrají hlavní roli v patogenezi alergického asthma.
Degranulace žírných buněk kolem cév má dva účinky: zvyšování permeability cévní stěny, vazodilatace. Mediátory obsažené v granulích žírných buněk přímo působí na buňky endotelu a způsobují jejich kontrakci. Tím vznikají mezi buňkami mezery, což vede ke zvýšení propustnosti stěny. Zároveň tyto mediátory stimulují produkci látek s vazodilatačním účinkem. Tyto dva mechanismy společně hrají roli v patogenezi anafylaxe.
Mediátory granulí žírných buněk ale ovlivňují také angiogenezi a řada z nich působí pro-angiogenně. Předpokládá se i role žírných buněk v angiogenezi při růstu tumorů. Při systémové hypoxii mají žírné buňky úlohu v rozvoji mikrovaskulárního zánětu. Při ischemizaci orgánů nebo při reperfúzi orgánů během transplantace pak stabilizace mastocytů vede ke snížení poškození orgánů.
Gastrointestinální trakt
V gastrointestinálním traktu se nachází velké množství slizničních žírných buněk. V případě, že se antigen naváže na žírné buňky, dochází k jeho prezentaci Th2 lymfocytům. Zároveň dochází k degranulaci žírných buněk a k vyvolání imunitní odpovědi. Žírné buňky tak plní funkci časné bariéry před vnikem patogenů. Mediátory vylité z granul žírných buněk způsobí zvýšení propustnosti cév ve střevním epitelu, čímž dojde k otoku sliznice a usnadnění průchodu tekutiny do střeva. Mediátory působí také na hladkou svalovinu, u které vyvolají kontrakci. Výsledkem je vyvolání zvracení a průjmu, což je jeden z obranných mechanismů proti parazitárním infekcím. Může se vyskytnout také kožní reakce (kopřivka, angioedém) v případě přenosu antigenu k žírným buňkám kůže. Produkce IgE proti neškodným antigenům, které jsou součástí potravy, se bude projevovat alergickou reakcí na dané potraviny.
Nosní sliznice, oči
Alergeny se mohou vázat na žírné buňky nacházející se ve sliznici nosu. Jejich aktivace vede ke klasickým symptomům alergické reakce: rýmě, slzení a nástřiku spojivek. Vazodilatace a zvýšení permeability cév ve sliznici způsobí otok sliznice a tím „ucpaný nos.“ Spolu s tím dochází k hypersekreci hlenu ze žláz. Na podkladě nervové stimulace histaminem (histamine-associate sensory neural stimulation) je vyvoláno kýchání.
Mast cell activation syndrome
Mast cell activation syndrom (MCAS) je stav, kdy na podkladě nefunkční vnitřní signalizace dochází k uvolňování neúměrně velkého množství mediátorů z žírných buněk. To může vést k řadě chronických symptomů nebo až k anafylaxi v případě systémové aktivace žírných buněk. Dermatologické symptomy mohou zahrnovat: zarudnutí, kopřivku, tvorba modřin, svědění, pálení, dermatografismus. Kardiologické symptomy: závratě, hypotenzní mdloby, ne-kardiogenní bolest na hrudi, arytmie, tachykardie. Gastrointestinální symptomy: průjem nebo zácpa, křeče, střevní diskomfort, nauzea, zvracení, kyselý reflux, problémy s polykáním. Neuropsychiatrické symptomy: bolest hlavy, únava, letargie, problémy se soustředěním, kognitivní deficit, poruchy spánku.
Možnosti ovlivnění žírných buněk
Farmakologické možnosti ovlivnění žírných buněk zahrnují zejména stabilizátory žírných buněk, H1 antihistaminika a antileukotrieny. Stabilizátory brání degranulaci žírných buněk a tím vylití obsahu granul. Jedním z možných mechanismů účinku je blokování IgE-regulovaného vápníkového kanálu. Do této skupiny léků patří například ketotifen, chromoglykát, vitamín D nebo β2 agonisté. H1 antihistaminika blokují H1 histaminový receptor na povrchu žírných buněk, čímž brání amplifikaci zánětlivé odpovědi. Tyto přípravky jsou hojně využívány pro ovlivnění alergické reakce, patří sem například cetirizin nebo levocetirizin.
Jinou možností ovlivnění žírných buněk je jejich desensitizace. Při úspěšné terapii dochází ke snížení množství FcεR1 receptorů na povrchu žírných buněk prostřednictvím opakované expozice nízkým dávkám antigenu.